
������1����С��1��ʷ���1���� ��1��2*��������1��2
��1����ũ�ֿƼ���ѧ��ѧԺ,���� ���� 712100;2����ʡƻ�����̼����о�����,���� ���� 712100��
ժҪ��Ϊʵ�ֶ�ƻ��Ʒ�ֿ���ȷ�ļ�������40�ݹ���������ƻ��Ʒ��Ϊ������ϣ�����6�����Ծ۱�ϩ����������Ӿ�����SSRӫ����ëϸ�ܵ�Ӿ������ϵķ�������ƻ��Ʒ�ֵ�SSR���ӱ��ָ��ͼ�����ݿ⡣(1) ѡ�þ��ȷֲ���17��Ⱦɫ���ϵ�144��SSR�������PCR��������Ӿ��⣬����PCR������ϵ�������˻��¶Ƚ����Ż���ɸѡ��35�Զ�̬�Խϸߡ��״�������������������35�����ﹲ��314����λλ�㣬ÿ��SSR������������λλ����3��15����ƽ��8.97������̬����Ϣ����ָ��(PIC)�仯��ΧΪ0.4553��0.8346��ƽ��Ϊ0.6920������λ����Ӻ϶���0.4750��1.0000֮�䣬ƽ��Ϊ0.7943�����ϵ��(MI)ƽ��Ϊ6.2080������CH04c10�����ƻ��������DNA����������Ч�����̬����Ϣ����ָ���ͱ��ָ������ߣ��ֱ�Ϊ0.8346��12.5190��(2) CH03d07��NZ02b1��CH05c04�������������ϼ������ɽ�40��ƻ��Ʒ����ȫ���ֿ�����(3) ӫ����ëϸ�ܵ�Ӿ����6�����Ծ۱�ϩ����������Ӿ����ܸ���ȷ����Ŀ��Ƭ�εĴ�С�����Ч����Ϊ���룬���ʺ���DNAָ��ͼ�����ݿ�Ľ����������������������ַ�����Ϲ���ƻ��Ʒ��DNAָ�Ƽ����������ȷ�����ɿ���
�ؼ�����ƻ��;SSR���;ӫ����;ָ��ͼ��
Establishment of SSR fingerprinting database on major cultivars of apple(Malus domestica)
WANG Li-xin1,Zhang Xiao-jun1,Shi Xing-yun1,Gao Hua1,2*,Zhao Zheng-yang1,2*
��1College of Horticulture��Northwest A&F University��Yangling��Shaanxi 712100��China��2Apple E&T Research Centre of Shaanxi Province��Yangling��Shaanxi 712100��China��
Abstract: In order to identify apple cultivars accurately, we established SSR fingerprinting database on 40 major cultivars of domestic and overseas apples through using the combine methods of 6% denaturing polyacrylamide gel electrophoresis detection and capillary electrophoresis detection with fluorescent SSR markers. 144 pairs of SSR primers which were chosen from 17 chromosomes were used to proceed with PCR amplification and electrophoresis. The PCR amplification system and primer annealing temperature were optimized and lastly 35 pairs of SSR primers which could amplify stable and distinct bands were screened. Results showed that the 35 pairs of SSR primers amplified a total of 314 alleles. Alleles amplified by each pair of primers ranged from 3 to 15, with a mean of 8.97. The polymorphic information content values (PIC) ranged from 0.4553 to 0.8346, with a mean of 0.6920. The heterozygosity ranged from 0.4750 to 1.0000, with a mean of 0.7943. The average of marker index (MI) is 6.2080 and the locus CH04c10 was effective to detect DNA variation . The highest value of PIC and MI was 0.8346 and 12.5190, respectively. The combination of locus CH03d07, NZ02b1and CH05c04 could identify the forty apple cultivars separately. Comparing with 6% denaturing polyacrylamide gel electrophoresis detection, the method of capillary electrophoresis detection with fluorescent SSR markers could detect target segments more accurately and ideally. It was more suitable used to establish SSR fingerprinting database. All in all, using the two methods to establish SSR fingerprinting database is accurate and reliable.
Key words��apple��SSR marker��fluorescent marker��fingerprinting
DNAָ��ͼ���ж�λ���ԡ��߱����ԡ����ȶ����Ŵ��ԣ�������䵮�������������ǵ����ӣ����ֳ����ʵ�ü�ֵ[16]���������������DNAָ��ͼ�����ݿ����Ʒ�ּ�����Ϊ���ӡ�Ӣ�����¹����������������������������1997��������һ������SSR��Ǽ�������С������������Ҫ����Ʒ�ּ�������Ŀ���ƶ���ͳһ�����÷��ӱ�Ǽ�������Ʒ�ּ����ķ�����������ũ�ֿ�ѧԺ�����о������ѽ����˻���SSR��Ǽ���������ָ��ͼ�����ݿ�[12]������������Ʒ�������Ѵ�5000��ݡ�����ֲ����Ʒ�ֱ������ˣ�UPOV���ѽ�SSR��Ǽ����͵��������̬�Լ�����SNP���Ƽ�Ϊ�ʺϹ���ָ��ͼ�����ݿ�����ּ�������ΪSSR��Ǽ�����Ŀǰ��Ϊ����ļ���[5]��
Ŀǰ���������SSRָ��ͼ�ķ����������֬�ǡ���ͨ�۱�ϩ�������������Ծ۱�ϩ����������Ӿ��TP-M13-SSR�����ͳ���ӫ��SSR�������ӷֱ����Ͽ����DZ��Ծ۱�ϩ�������������ֱܷ��С��2����������ڵIJ��죬��֬�������ֱ��ʸ��ͣ������Ծ۱�ϩ����������Ӿ��Ϸ�������Ӱ����Ⱦ���ֶ��ܹ��ֱ���СΪ1������ԵIJ��죬�ܹ��ֱ�ͬһSSRλ���ϵIJ�ͬ��λ������ȫ���㹹��ָ��ͼ�����ݿ�Ե�λ�����С�ֱ��ʵ�Ҫ����DNA�����ǵ�SSRӫ����ëϸ�ܵ�Ӿ��ⷽ�����Եõ�������DNAƬ�η������ݣ��볣��ľ۱�ϩ����������Ӿ��ⷽ����ȣ�ëϸ�ܵ�Ӿ�������Ϊ��ȷ����������Ч���������ڴ�����Ʒ�ֵļ�����[13]��������ñ��Ծ۱�ϩ����������Ӿ�����SSRӫ����ëϸ�ܵ�Ӿ��ⷽ�����ϵķ�������ƻ��Ʒ��DNAָ�Ƽ������������С�����ɿ�[3]��
ƻ����������Դ�ḻ������ࡢ�ֲ�������������ʷ�ƾ����ڹ������ࡢ�����������Ͼ��ü�ֵ�ܸ�[6-7]�����Ź������ּ����IJ��Ϸ�չ������������ƻ������Ʒ��Խ��Խ�࣬��֤Ʒ�ֵ���ʵ�ԡ�ά�������������ּҵ�Ȩ���Ե�������Ҫ����ƻ���������Է�ֳ����������߶��Ӻϣ��������ͬ��������ͬ������������������Ϊ���ѡ�������Ʒ�ּ�����Ҫ����ָ̬�꣬�����ڲ��첢�����Եĸ��壬��ͳ����̬��������ʶ�𣬶����÷��ӱ�ǣ�SSR ����Ʒ�ֽ��м����ͷ���[8]����һ�ּ�ȷ���ҿɿ��ķ�������˹���ƻ��SSRָ��ͼ�����ݿ��ƻ��Ʒ�ּ��������Ҫ���塣
1 �����뷽��
1.1������
����ƻ��Ʒ�ֹ�40��(��1)����ȡ������ũ�ֿƼ���ѧ��ˮƻ������վƷ����Դ�ԡ��ڴ���ȡ������Ҷ�����ک�80���±��á�
��1 ���Ե�ƻ��Ʒ��
Table 1 Apple cultivars used in this study
|
���
No. |
Ʒ��
Variety |
�ױ�
Parent |
���
No. |
Ʒ��
Variety |
�ױ�
Parent |
|
1 |
���ɽ�Jonagold |
���������GoldenDelicious��Jonathan |
21 |
����Huacui |
�������Golden Delicious��Megumi |
|
2 |
���Golden Delicious |
unknown |
22 |
��˶Huashuo |
�����˺�������American number eight��Huaguan |
|
3 |
������ƻGranny Smith |
unknown |
23 |
ǧ��Senshu |
��������ʿToko��Fuji |
|
4 |
����Qinyang |
����ʵ��Seeding of Gala |
24 |
����Xiayan |
���⣨�º�������ڣ�Rall��(Starkrinson��Hongguan�� |
|
5 |
����Ralls |
unknown |
25 |
����һSekaiichi |
Ԫ˧�����Delicious��Golden Delicious |
|
6 |
ɺ��Sansa |
��������Gala��Akane |
26 |
ӭ��Yingqiu |
������ף��Jonathan��Summer pearmain |
|
7 |
��Ũ��Xinnonghong |
����������Tsugaru��Bella |
27 |
����Jinhong |
����������Jonathan��Jiguan |
|
8 |
�ɱ���Songbenjin |
unknown |
28 |
���Dailv |
���ʵ��Seeding of Golden Delicious |
|
9 |
����Toko |
�����ӡ��Golden Delicious��Indo |
29 |
����ŷCameo |
Red Delicious��Golden Delicious |
|
10 |
��¶Tallman's Sweet |
unknown |
30 |
�챦ʯHongbaoshi |
������Ԫ˧Ralls��Delicious |
|
11 |
����Qinyan |
���������ع�Tianwanghong��Qinguan |
31 |
Ħ��ʿMollie's Deli |
unknown |
|
12 |
����Northern Spy |
unknown |
32 |
̩ɽ��ϼTaishanZaoxia |
���ʵ�� Seeding of Geneva Early |
|
13 |
����Huajin |
unknown |
33 |
��Kizashi |
��������ʿGala��Fuji |
|
14 |
������Jinshiji |
����ѿ��Sport of Gala |
34 |
���Qiujin |
��������ϻ���Ralls��Pollen mixture |
|
15 |
��ƿ�Tianhuangkui |
ף�����ƿ�Summer Pearmain��YellowTransparent |
35 |
����Ben Davis |
unknown |
|
16 |
���¶Honggailu |
����ѿ��Sport of Gala |
36 |
��ϼDanxia |
���ʵ��Seeding of Golden Delicious |
|
17 |
����Hokudo |
��ʿ��½��Fuji��Mutsu |
37 |
�Ϸ���GS330 |
����������Gala��Huali |
|
18 |
�º���Starkrinson |
����ѿ��Spot of Red delicious |
38 |
����Qinxing |
�º������ع�Starkrinson��Qinguan |
|
19 |
½��Mutsu |
�����ӡ��Golden Delicious��Indo |
39 |
���Geneva Early |
Quitd�����º�Quitd��Qiyuehong |
|
20 |
����Liberty |
unknown |
40 |
�����Hongjinfu |
��ʿѿ��Sport of Fuji |
1.2 ����
1.2.1 DNA��ȡ
�ο����ȷ�������ȡƻ��ҶƬ������DNA��������֬��������Ӿ�����������������ֹ��ȼ�ND��2000�ⶨ������Ũ�ȣ����ս�DNA��Ʒϡ����80 mg��L-1���á�
1.2.2 ����ϳ�
�ο���վ��http://www.hidras.unimi.it/�����Ϻ����﹤������˾�ϳ�144����ͨSSR�����ɸѡ��35��ӫ������5���˷ֱ���FAM��HEX��TAMRA��ROX 4ɫӫ��Ⱦ�ϱ��(��2)�����Ϻ����﹤������˾�ϳɡ�
1.2.3 PCR����
15µL�ķ�Ӧ�������ÿ��dNTP 0.20mmol/L����������0.27mmol/L����������0.27mmol/L��Taq DNA�ۺ�ø1U��1��PCR����Һ(����Mg2+)��MgCl2 1.5 mmol/L����ƷDNA 6 ng/µL��
��Ӧ����94��Ԥ����4min��94������45s��Tm��(�������)����45s��72������50s��35��ѭ����72������10min��4��������
1.2.4���Ծ۱�ϩ����������Ӿ��ӫ����
PCR ���������м���6��L Loading buffer (98%��������pH 8.0��10mmol/L EDTA��0.25%�������0.25%���ױ���)��95������5min��������ȴ����6 %�ı��Ծ۱�ϩ���������ϵ�Ӿ50min ����(80W �㹦�ʣ�����Ԥ��Ӿ30min) ����Ⱦ����������
��5'FAMӫ���ǵ�PCR�����ó���ˮϡ��30����HEXӫ���ǵ�PCR����ϡ��15����TAMRAӫ���ǵ�PCR����ϡ��10����ROXӫ���ǵ�PCR����ϡ��5�����ֱ�ȡ�����������4��ϡ�ͺ���Һ��ϣ��ӻ��Һ����ȡ1 mL���뵽DNA������ר����װ���С����и�������0.5mL LIZ500�������ڱ��8.5mLȥ���Ӽ���������������Ʒ�⣬��Ӧͬʱ��������Ʒ�������������Ʒ��PCR����95������5min������ȡ�����ڱ��ϣ���ȴ10 min���ϡ�˲ʱ����10 s���ϻ���Ӿ��
1.2.5 ��Ӿ���ݷ���
ʹ��Genemapper4.0�����ռ�ԭʼ���ݣ�������Power Marker V3.25�Թ��Բ��Ͻ��з�����������ַ�����õĵ�λ�������ݽ���ͳ�ƣ��Ա��������
2 ��������
2.1 PCR������ϵ�������˻��¶�
���Ż����������ʺ�ƻ��SSR����PCR������ϵ(������3.2.3)��35��ӫ�����������˻��¶ȣ�����2����
��2 ɸѡ����35�Ժ������ӫ�������ͼ�����˻��¶�
Table 2 35 pairs of screened microsatellite primers, type of fluorescence and optimum annealing temperature
|
��������
Primer name
|
ӫ��
Fluorescence
|
�˻��¶�Annealing
Temperature/�� |
��������
Primer name
|
ӫ��
Fluorescence
|
�˻��¶�Annealing
Temperature/�� |
|
NZ02b1 |
5'FAM |
53 |
CH01f03b |
5'HEX |
56 |
|
CH03d07 |
5'FAM |
48 |
Hi12c02 |
5'TAMRA |
57 |
|
CH01d08 |
5'FAM |
53 |
CH04c10 |
5'TAMRA |
54 |
|
CH04e03 |
5'FAM |
54 |
CH05g03 |
5'TAMRA |
54 |
|
CH02d08 |
5'FAM |
57 |
CH04d08 |
5'TAMRA |
49 |
|
Hi02d04 |
5'FAM |
54 |
CH04g12 |
5'TAMRA |
54 |
|
Hi22f06 |
5'FAM |
55 |
CH02c02a |
5'TAMRA |
56 |
|
CH02c09 |
5'FAM |
55 |
CH04e02 |
5'TAMRA |
54 |
|
CH04f10 |
5'FAM |
50 |
CH04g07 |
5'TAMRA |
55 |
|
CH05d03 |
5'FAM |
55 |
CH05e06 |
5'TAMRA |
55 |
|
CH05c04 |
5'HEX |
53 |
CH05c07 |
5'ROX |
52 |
|
CH04a12 |
5'HEX |
53 |
CH02g09 |
5'ROX |
53 |
|
Hi04g05 |
5'HEX |
54 |
CH03d12 |
5'ROX |
53 |
|
CH01g05 |
5'HEX |
58 |
CH01f09 |
5'ROX |
54 |
|
Hi03c05 |
5'HEX |
53 |
Hi03d06 |
5'ROX |
53 |
|
Hi03eo3 |
5'HEX |
56 |
CH04d02 |
5'ROX |
56 |
|
CH01f07a |
5'HEX |
56 |
Hi02c07 |
5'ROX |
56 |
|
CH04e05 |
5'HEX |
54 |
|
|
|
2.2 ���������ɸѡ��SSR��̬��
ѡ�þ��ȷֲ���ƻ��17��Ⱦɫ���ϵ�144��SSR�������8��ƻ�����Ͻ���PCR��������Ӿ��⣬����PCR������ϵ�������˻��¶Ƚ����Ż���ɸѡ��35�Զ�̬�Ըߡ��״����������Ȼ����35�������40�ݲ����������ֱ����6�����Ծ۱�ϩ����������Ӿ�����SSRӫ����ëϸ�ܵ�Ӿ��⣬�����ݽ���ͳ�Ʒ�����õ�40�ݲ�����35��λ�������(��2)35�����ﹲ��314����λλ�㣬ÿ��SSR������������λλ����3��15����ƽ��8.97������̬����Ϣ����ָ�� (PIC) �仯��ΧΪ0.4553��0.8346��ƽ��Ϊ0.6920������λ����Ӻ϶���0.4750��1.0000֮�䣬ƽ��Ϊ0.7943�����ϵ�� (MI) ƽ��Ϊ6.2080 ������CH04c10�����ƻ��������DNA����������Ч�����̬����Ϣ����ָ���ͱ��ָ������ߣ��ֱ�Ϊ0.8346��12.5190������ѡ35��������PIC��0.5�ĸ߶ȶ�̬����Ϣ����33�ԣ�0.25��PIC��0.5���жȶ�̬����Ϣ����2�� (CH01f09, 0.4622; Hi03e03, 0.4553)��
�� 3 35��SSRλ����40��ƻ��Ʒ���ϼ����Ŵ�������
Table 3 Genetic diversity of 40 cultivars revealed by 35 SSR primers
|
���Marker |
����λ����Ƶ��
Major Allele Frequency |
��������
Genotype No. |
�������Allele No. |
���������
Gene Diversity |
�Ӻ϶�
Heterozygosity |
��̬����Ϣ����
PIC |
���ϵ��
MI |
|
CH01d08 |
0.3375 |
9 |
5 |
0.7459 |
0.9500 |
0.7017 |
3.5083 |
|
Hi04g05 |
0.3250 |
18 |
9 |
0.7959 |
0.8000 |
0.7697 |
6.9274 |
|
CH04g12 |
0.3158 |
17 |
12 |
0.7822 |
0.9737 |
0.7533 |
9.0398 |
|
Hi03d06 |
0.5946 |
13 |
8 |
0.6019 |
0.5946 |
0.5694 |
4.5556 |
|
CH02d08 |
0.3500 |
20 |
12 |
0.8000 |
0.7750 |
0.7769 |
9.3224 |
|
Hi03c05 |
0.2750 |
20 |
11 |
0.8269 |
0.9500 |
0.8056 |
8.8621 |
|
CH01f09 |
0.6125 |
6 |
5 |
0.5322 |
0.6750 |
0.4622 |
2.3109 |
|
Hi02d04 |
0.2500 |
17 |
11 |
0.8403 |
1.0000 |
0.8210 |
9.0306 |
|
Hi03e03 |
0.7125 |
10 |
9 |
0.4741 |
0.4750 |
0.4553 |
4.0980 |
|
CH05g03 |
0.4000 |
12 |
10 |
0.6819 |
0.9750 |
0.6288 |
6.2884 |
|
CH03d12 |
0.4875 |
12 |
10 |
0.6775 |
0.6500 |
0.6339 |
6.3385 |
|
NZ02b1 |
0.3590 |
11 |
7 |
0.7094 |
0.8462 |
0.6562 |
4.5932 |
|
CH05c04 |
0.3000 |
16 |
10 |
0.7984 |
0.9750 |
0.7711 |
7.7112 |
|
Hi12c02 |
0.4103 |
9 |
6 |
0.6769 |
0.5897 |
0.6179 |
3.7076 |
|
CH05c07 |
0.4079 |
15 |
11 |
0.7687 |
0.8947 |
0.7446 |
8.1906 |
|
CH03d07 |
0.3625 |
18 |
10 |
0.7663 |
0.7250 |
0.7332 |
7.3316 |
|
CH04a12 |
0.4189 |
15 |
10 |
0.7684 |
0.8108 |
0.7464 |
7.4640 |
|
CH04c10 |
0.2564 |
21 |
15 |
0.8498 |
0.6154 |
0.8346 |
12.5190 |
|
CH02g09 |
0.3784 |
12 |
7 |
0.7359 |
0.8108 |
0.6951 |
4.8654 |
|
CH04e03 |
0.4474 |
16 |
10 |
0.7029 |
0.6842 |
0.6618 |
6.6180 |
|
CH01g05 |
0.3750 |
12 |
8 |
0.7341 |
0.8250 |
0.6909 |
5.5271 |
|
CH04d08 |
0.2125 |
20 |
9 |
0.8388 |
0.8250 |
0.8184 |
7.3656 |
|
Hi22f06 |
0.5375 |
6 |
3 |
0.5816 |
0.7250 |
0.5032 |
1.5095 |
|
CH01f07a |
0.3000 |
16 |
9 |
0.8078 |
0.8500 |
0.7825 |
7.0422 |
|
CH02c02a |
0.2895 |
24 |
14 |
0.8380 |
0.7895 |
0.8210 |
11.4935 |
|
CH04d02 |
0.4625 |
7 |
5 |
0.7022 |
0.9250 |
0.6619 |
3.3094 |
|
CH02c09 |
0.3000 |
14 |
8 |
0.7872 |
0.9000 |
0.7559 |
6.0469 |
|
CH04e05 |
0.5769 |
11 |
9 |
0.6203 |
0.6667 |
0.5881 |
5.2928 |
|
CH04e02 |
0.4875 |
11 |
7 |
0.6853 |
0.7000 |
0.6449 |
4.5141 |
|
Hi02c07 |
0.4125 |
10 |
7 |
0.6753 |
1.0000 |
0.6187 |
4.3311 |
|
CH04f10 |
0.2750 |
19 |
11 |
0.7978 |
0.8500 |
0.7684 |
8.4528 |
|
CH04g07 |
0.5000 |
12 |
10 |
0.7022 |
0.8158 |
0.6768 |
6.7681 |
|
CH05d03 |
0.4375 |
15 |
9 |
0.7216 |
0.6750 |
0.6855 |
6.1695 |
|
CH01f03b |
0.3375 |
15 |
9 |
0.7716 |
0.8000 |
0.7390 |
6.6512 |
|
CH05e06 |
0.5526 |
10 |
8 |
0.6524 |
0.6842 |
0.6253 |
5.0022 |
|
ƽ��
Mean |
0.4016 |
14 |
9 |
0.7272 |
0.7943 |
0.6920 |
6.2080 |
2.3 ָ��ͼ����
��������35�������40��ƻ������Ʒ�ֽ���ָ��ͼ������35�����ﶼֻ�ܽ�40��ƻ��Ʒ�ַ�Ϊ�������ͣ������κ�һ�����������ȫ����40��Ʒ�֡�����CH03d07��Ʒ��1��3��4��6��9��20��24��33��34��35��36��37�Ͼ�����������������������Ʒ�����ֿ�������Ʒ��2��11��31��39 ������ͬ��Ʒ��5��8��18��22��26��27��28��40������ͬ��Ʒ��7��10��15��16������ͬ��Ʒ��12��13��19��21��25��29������ͬ��Ʒ��14��32������ͬ��Ʒ��17��23��30��38������ͬ����������35����������ѡ��̬����Էḻ�����������ϼ�����ȫ����40��Ʒ�֣���CH03d07��NZ02b1��CH05c04���ɽ�40����Ʒ����ȫ���ֿ���
2.4 ����ëϸ�ܵ�Ӿ�������Ծ۱�ϩ����������Ӿ���Աȣ��ۺ��������ַ�����
Ϊ�˼���6�����Ծ۱�ϩ����������Ӿ��ⷽ���Ŀɿ��ԣ���ӫ����ëϸ�ܵ�Ӿ��ⷽ����40�����������35��SSR������������ָ�����ݽ�������֤��������ַ������ĵ�λ������Ŀ��ʵ����϶�Ӧ�ĵ�λ�������ͻ���һ��(ͼ1��ͼ2����ֻ����������������Ʒ����ӫ����ëϸ�ܵ�Ӿ���ȱ��Ծ۱�ϩ����������Ӿ�����1����λ����(ͼ1��ͼ3����
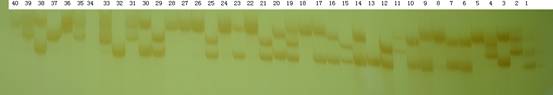
ͼ 1 ����CH03d07��40��ƻ������Ʒ�ֵ��������
1��40��Ʒ�ֱ��ͬ��3
Figure 1 DNA fragments amplified by SSR primer CH03d07 in 40 persimmon major cultivars
1��40��The codes of varieties are same as Table 3
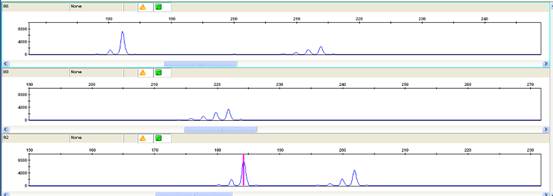
ͼ 2 ӫ������CH03d07��16�ţ�8�ź�12�ţ��������£�ƻ��Ʒ���ϵ�ëϸ�ܵ�Ӿ���͡�
Figure 2 Capillary electrophoresis profiless of the sixteenth, eighth and twelfth apple materials(From up to down) at fluorescent primer CH03d07
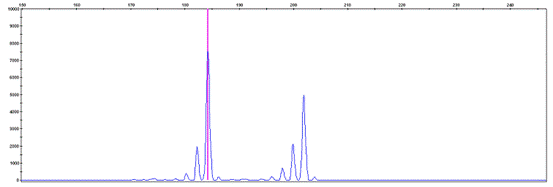
ͼ 3 ӫ������CH03d07��13��ƻ��Ʒ���ϵ�ëϸ�ܵ�Ӿ���͡�
Figure 3 Capillary electrophoresis profiless of the thirteenth apple material at fluorescent primer CH03d07
3 ����������
���о�ƻ��ָ��ͼ��PCR������ϵ���Ż����̿�֪SSR�Է�Ӧ��ϵҪ��dz��ϸ������Ƕ�ƻ�����ָ߶��Ӻϵ����֣��ڷ�Ӧ��ϵ��������Mg2+���ֳɷֺ����仯����������Ӱ��ϴ�[1,10]�����Mg2+Ũ�����Ӿ��ᵼ�´����������������ij��֣�������SSR������������ָ��ͼ��Ҫ���������������ȶ����������Ըߣ���˶�PCR��Ӧ��ϵ���Ż������ָ��ͼ������ǰ�ᡣ���о�ͨ������ʵ��̽����һ���ȶ�������ƻ��SSR��������ϵ�����Ϊ���������Ľ��е춨�˻�����
ѡ����ʵ������ǹ���ƻ������ָ��ͼ����һ��Ҫǰ��[14-15]�����о�ѡȡ��144��SSR�������λ��ƻ��17��Ⱦɫ���ϡ��ڶ�144��SSR������ж��ɸѡ�Ļ����ϣ�ɸѡ��35�Զ�̬�Ըߡ��ظ��Ժõ��������ͼ�����������ݷ����з��֣���ͬ�������Ʒ�ּ��̬�Եļ��������нϴ���죬���κ�һ�����������ȫ����40��Ʒ�֡�����35����������ֱ���к�����3��4��������Ϻ��֣�ÿ����Ͽ��Խ����й��Բ������ֿ������ͨ����ͬ�����������ϣ����Դ���������ļ���������������Ʒ�������Ľ�һ�����ӣ��������ϻ�����Ҫ��һ���Ӵ������ϵ�ƻ������Ʒ���м�ǧ�֣��������е�ƻ������Ʒ�ֻ������Ʒ��ʱ����������ͬһ�����ڲ�ͬƷ�ּ������ͬ�״�������ʱӦ���ò�ͬ�ĺ���������ϻ���ɸѡ�µ�SSR���ォ�����ֿ����Բ������չ���ѽ����ij���ָ��ͼ�ס�
�ڲ���SSR�۱�ϩ����������Ӿ��ⷽ������ƻ��Ʒ��DNA���ݿ�Ĺ����У����ȷ�����ϲ�ͬ���Ρ���ͬ�����ƻ��Ʒ��DNAָ�Ƽ�������һֱ�Ǹ�����[17]��Ϊ�˱�֤ƻ��Ʒ��DNAָ��ͼ�����Ŀ����������Ŀɿ��ԣ����о�������6�����Ծ۱�ϩ����������Ӿ��ⷽ����SSR���ëϸ�ܵ�Ӿ��ⷽ�����Ͻ�����֤���볣���������Ӿ��ⷽ����ȣ�ӫ����ëϸ�ܵ�Ӿ������ݸ�Ϊ��ȷ��ͬʱ�ܺõؽ���˴��ģ��ͬ����DNAָ�Ƽ���������Ч���Ϻ�ȷ�Ƚϵ����⡣���Ҷ���ëϸ�ܵ�Ӿ�������Գɱ�����Ч�ʣ����һ������������ͼ��ɱ������о����֤�����ַ������ĵ�λ������Ŀ��ʵ����϶�Ӧ�ĵ�λ�������ͻ���һ�¡�
����� :
[1] Luis G, Cristina M, Oliveira. Molecular characterization of cultivars of apple (Malus domestica Borkh.) using microsatellite(SSR and ISSR) markers [J]. Euphytica, 2001, 122��81-89.
[2] Tautz D. Hyper variability of simple sequences as a generalsource for polymorphic DNA markers [J]. Nuleic AcidsRes, 1989, 17(16)��6463-6471.
[3] Takezak I N, Nei M. Genetic distances and reconstruction of phylogenetic trees from microsatellite DNA [J]. Genetics, 1996, 144��389-399.
[4] Liebhard R, Gianfranceschi L, Koller B, Ryder C D, Tarchini R, Van De, Weg E. And Gessler C. Development and characterisation of 140 new microsatellites in apple (Malus��domestica Borkh.). Molecular Breeding, 2002, 10��217-241.
[5] �� ��. ƻ������Ʒ�ֵ�DNAָ��ͼ�������Ŵ������Է��� [D]. ���裺����ũ�ֿƼ���ѧ. 2010.
[6] �� Դ, ����֮, �����, ��. ƻ����������Դ��Ե��ϵ��SSR���� [J]. ����ѧ��, 2007, 24(2)��129-134.
[7] ������, ������, ��ѩ��, ��. ƻ��Ʒ�ֵ�SSR ���� [J]. ��ѧ��, 2005, 32(5)��875-877.
[8] Guiford P, Prakash S, Zhu J M. Microsatellites in Malus domestica(apple): abundance, polymorphism and cultivar identi- fication [J]. Theor Appl Genet, 1997, 94��249-254.
[9] �� Դ, �� ��, ��·��, �����, ��. Ӧ��TP-M13-SSR ��������ƻ��Ʒ�� [J].����ѧ��, 2010, 27(5)��833-837.
[10] �� ��, ������. ƻ������Ʒ�ֵ�SSR���ӱ�Ǽ��� [J]. �й�ũѧͨ��, 2007, 129-134.
[11] �� Դ, �� ��, ��·��, ��. TP-M13-SSR����������ƻ��������Դ�Ŵ��������о��е�Ӧ�� [J]. ֲ���Ŵ���Դѧ��, 2011, 12( 2)��228-233.
[12] �����, �Ծ�Ȼ, ������.�й�������Ʒ��DNA�⽨��ϵ���о���I. ����Ʒ�ִ��ȼ���α������SSR��ʵ����ϵ�Ľ��� [J]. ����ѧ, 2003, 11(1)��3-6.
[13] �³���, ������, �ּ���. SSR��Ǻ���Ⱦ�����ıȽϷ��� [J]. ����ѧ��, 2005, 31(2)��144-149.
[14] �� �, ������, �� �.�����Ʒ�ֵ�SSRָ��ͼ�Ĺ��� [J]. ��ѧ��, 2011, 38(1)��159�C164.
[15] ������, ��־��, �ռ���, ��. 32��������Ʒ��SSR�������Ŵ�������� [J]. ����ֲ��ѧ��, 2011, 31(11)��2185-2191.
[16] ��׳ΰ, �� ��. 38��ŷ����ݮ����Ʒ��SSRָ��ͼ�Ĺ��� [J]. ����ѧ��, 2011, 28(6)�� 1032-1037.
[17] �̱���, �Ŀ���, ������, ���˻�. ��ëϸ�ܵ�Ӿ��ⷨ��ˮ��DNA�����е�Ӧ�� [J]. �й�ˮ����ѧ, 2011, 25(6)��672-676.
����飺�����£�1987-�����У��ӱ������ˣ�˶ʿ�о������о�����Ϊ�������������\����
ͨѶ���ߣ�����1970-�����У������Ӱ��ˣ����о�Ա��˶ʿ����Ҫ����ƻ����Ʒ��ѡ�����������༼���о���ʾ���ƹ㹤������������1964-�����У�����μ���ˣ����ڣ���ʿ����Ҫ���³������֡���������ѧ���ֵȡ�

